轰轰烈烈的一部病毒性肝炎药物发展史,也是半部病毒性肝炎消亡史。
2022年5月,第75届世界卫生大会通过了《2022-2030年全球卫生部门关于艾滋病、病毒性肝炎和性传播疾病行动计划》(简称《2022-2030行动计划》)决议[1],对2016年大会通过的关于消除病毒性肝炎策略进行了修订,不仅提出了更具体的目标,更在国家层面给出了可量化指标。
病毒性肝炎主要包括丙肝和乙肝,目前丙肝已经宣告90%以上的治愈率,乙肝的治愈率也随着诊疗方案的改进不断有新的突破,消除病毒性肝炎目标进入倒计时。
我们试着从丙肝和乙肝疾病的“消除计划”,走进相关治疗药物的发展史。
01
一场事关全球的“行动计划”
《2020-2030行动计划》提出的目标,仍然是到2030年消除病毒性肝炎的公共卫生威胁,即以2015年为基础,到2030年慢性乙型肝炎(CHB)和慢性丙型肝炎(CHC)新发感染率下降90%,死亡率降低65%,但今年提出了更具体的指标。
乙肝目标:CHB新发病由2020年150万例(20/10万),2025年降至85万例(11/10万),2030年降至17万例(2/10万);CHB死亡由2020年82万例(10/10万),2025年降至53万例(7/10万),2030年降至31万例(4/10万)。
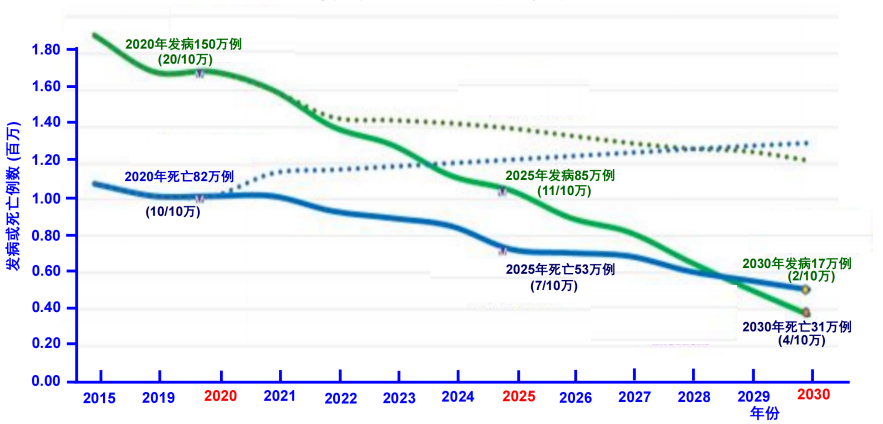
图1《2020-2030行动计划》对乙型肝炎发病率和死亡率的目标
图片来源:《2022-2030年全球卫生部门关于艾滋病、病毒性肝炎和性传播疾病行动计划》
丙肝目标:新发病由2020年157.5万例(20/10万),2025年降至100万例(13/10万),2030年降至35万例(5/10万);CHC死亡由2020年29万例(5/10万),2025年降至24万例(3/10万),2030年降至14万例(2/10万)。
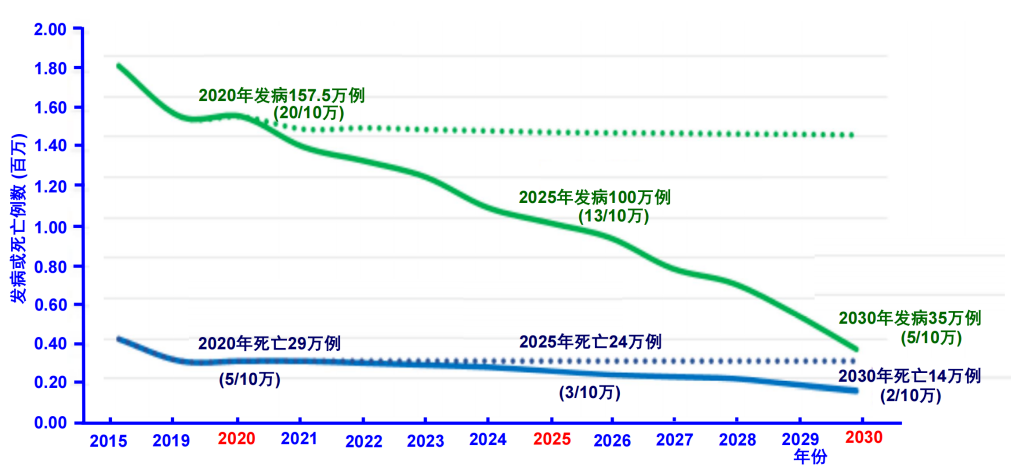
图2《2020-2030行动计划》对丙型肝炎发病率和死亡率的目标
图片来源:《2022-2030年全球卫生部门关于艾滋病、病毒性肝炎和性传播疾病行动计划》
值得注意的是,关于《2020-2030行动计划》提出的七项关键措施指标,全球现有数据情况不容乐观。
根据2020年发布的Polaris报告[2],全球首针乙型肝炎疫苗接种率仅为49.1%;我国首针乙型肝炎疫苗接种率和3针乙肝疫苗覆盖率已超过全球数据,并已经达到WHO 2030年指标,但我国乙型肝炎诊断率为22%,治疗率仅为17%,距离WHO 2020年目标(30%/30%)都仍有很大距离。
在丙型肝炎(丙肝)方面,形势同样严峻。
Polaris的报告数据显示,虽然全球和我国的丙肝诊断率达到了2020年30%的目标,但全球丙肝治疗率仅为15%,我国只有10%,远未达到2020年30%的目标。
因此,消除病毒性肝炎,任重而道远。
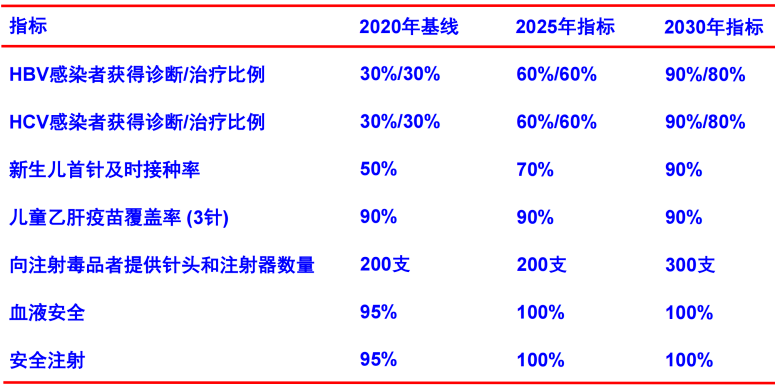
图3《2020-2030行动计划》2025/2030年消除病毒性肝炎关键措施指标
图片来源:《2022-2030年全球卫生部门关于艾滋病、病毒性肝炎和性传播疾病行动计划》
02
乙肝/丙肝患病率
及患者人群特点
乙肝一般指慢性乙型病毒性肝炎,指慢性乙肝病毒检测为阳性,病程超过半年或发病日期不明确而临床有慢性肝炎表现者。临床表现为乏力、畏食、恶心、腹胀、肝区疼痛等症状,严重可导致肝衰竭、肝硬化或肝癌。
丙肝则一般分为急性和慢性。急性可出现恶心,食欲下降,全身无力,尿黄眼黄等表现。成人在不进行抗病毒干预的情况下,85%的患者发展为慢性丙型肝炎,儿童则有50%可自发性清除HCV。慢性丙型肝炎症状较轻,表现为容易疲劳,食欲欠佳,腹胀等,严重可导致肝硬化或肝癌。
据WHO报道,2019年全球一般人群HBsAg流行率为3.8%,约有150万例新发HBV感染者,2.96亿例慢性HBV感染者(乙肝患者),82万例死于HBV感染所致的肝衰竭、肝硬化或HCC等相关疾病。根据Polaris国际流行病学合作组织推算,2016年我国一般人群HBsAg流行率为6.1%,慢性HBV感染者为8600万例。
据WHO报道,2015年全球有慢性HCV感染者(丙肝患者)7100万例,39.9万例死于HCV感染引起的肝硬化或HCC。2019年全球有慢性HCV感染者5800万例,29万例死于HCV感染引起的肝硬化或HCC;2019年全球新发感染者约150万例。根据Polaris数据,2020年我国HCV感染者接近950万例[4]。
“我大学毕业,面试的时候用人单位都说我是人才,一体检完就没信了。我尽力了,可是尽力有用吗?”这段感受出自吉利德科学公益支持的电影《不止不休》,改编自真实故事,以一名记者的成长史为切入口,折射出20年前乙肝患者和疾病、社会歧视作斗争的过程。目前虽然已经提倡全社会禁止歧视乙肝患者,但实际仍会受到不公正对待。
03
丙肝治疗药物发展历程
丙肝病毒共存在6种基因型,丙肝患者以基因1型居多,约占70%。制药企业开发的口服抗病毒药物主要针对靶点为其非结构蛋白NS3、NS4A、NS5A和NS5B。
最早上市的口服直接抗病毒药物(DAA)是NS3/4A蛋白酶抑制剂,包括波普瑞韦、特拉瑞韦、西美瑞韦。虽然NS3/4A蛋白酶抑制剂均需要与利巴韦林和干扰素注射联用,但由于将临床治愈率从40%提高到了80%以上,“干扰素注射+利巴韦林+DAA”还是成为丙肝的临床标准治疗方案而盛极一时。
2013年12月6日,吉利德旗下索磷布韦以“突破性药物”的身份获得FDA批准上市,为基因2,3型丙肝患者提供了一种不需要注射干扰素的纯口服治疗方案,而且治愈率在90%以上。此后,丙肝治疗进入索磷布韦时代,大家也将其奉为丙肝神药。天价收购、超高治愈率、铺天盖地的媒体宣传让索磷布韦在上市之前就被医生和患者熟知,即便是吉利德定了1000美元/片(84000美元/疗程)的高昂定价,也无法阻挡临床处方的热情。2014年,索磷布韦上市的第一年,销售收入102.83亿美元,创下新药上市第一年销售收入记录。
2014年,吉利德旗下Harvoni(索磷布韦/雷迪帕韦)美国上市,为患者数量最多的基因1型丙肝患者提供了纯口服治疗方案,而且治疗周期更短,治愈率更高。Harvoni获批上市2个多月便贡献21.27亿美元收入。同年,艾伯维的四合一丙肝新药Viekira Park(达塞布韦钠/奥比他韦/帕利瑞韦/利托那韦)获得FDA批准,之后不久又获得欧盟批准,因为同样是纯口服方案,治愈率也不相上下,吉利德迎来了竞争对手,医保支付方也终于有了和吉利德讨价还价的筹码。但如今看来,这款药没有逃脱撤市的命运。
2015年是吉利德把丙肝药业务做得最大的年份,也是暗藏危机的一年。索磷布韦销售额腰斩,纵然Harvoni全年销售成绩艳丽,但从季度销售收入上看,已经不再增长,毕竟全球的医疗卫生支出承受能力不可能无限放大。
2016年,默沙东的丙肝新药Zepatier(艾尔巴韦/格拉瑞韦)终于获得FDA批准上市,口服丙肝药时代最后一个巨头进场。默沙东出招凌厉,虽然时间上已经不占优势,但是会打价格战。同年,吉利德覆盖全基因型的丙肝产品Epclusa(索磷布韦/维帕他韦)美国上市,产品性能继续优化的空间已不大,加上丙肝患者日益减少,降价似乎成了最有效的出路。受患者减少和降价影响,2016年全球丙肝市场规模大约190亿美元,较2015年下降了30%以上。
2017年,吉利德和艾伯维分别推出全基因型丙肝药物Vosevi(索磷布韦/维帕他韦/伏西瑞韦)和Maviret(格卡瑞韦/哌仑他韦)。此后,吉利德更是表态不再投入资源开发丙肝新药。
至此,一个拥有庞大患者人群及及市场的疾病逐步走向消亡,关于丙肝药的头号玩家竞争也基本步入终局。此后,国产丙肝药,如歌礼制药旗下达诺瑞韦和拉维达韦,凯因科技旗下可洛派韦,东阳光药业旗下依米他韦也相继上市。
如今,丙通沙Epclusa一个疗程国内只需自付不到2000元,相比医保前一个疗程近7万的价格降低了97%,丙肝患者是最大的受益者。九部委联合发布的《消除丙型肝炎公共卫生危害行动工作方案(2021—2030年)》提出“我国丙肝患者抗病毒治疗的临床治愈率超过95%、慢性丙肝抗病毒治疗率超过80%”的目标,这与我国目前的实际情况仍有很大差距。
显然,未来几年,是多家丙肝药企业迫切需要抢占的时间窗口。
04
乙肝治疗药物发展历程
1990年,干扰素-α的发现,使得人们开启了乙肝治疗的新篇章。因为这个药物具有稳定可靠的抗病毒效果,能通过调节机体免疫力,使得被乙肝病毒感染的肝细胞得以免疫系统识别并消灭,从而起到治疗乙肝的作用。不过,干扰素-α属于短效干扰素,不够稳定、代谢快、需要每天都给药,比较麻烦,副作用较大,效果也不是很理想。
到了1998年,葛兰素史克研发出了第一款口服抗病毒药物—拉米夫定,它是一种核苷类似物,对乙肝病毒具有良好的抑制效果,但同时也出现了耐药问题。为了克服这个问题,该公司又研发的一款核苷药—阿德福韦酯,它能在一定程度上克服拉米夫定的耐药问题,但它的肾毒性较大,同样无法满足广大乙肝患者的需求。
2005年,百时美施贵宝旗下核苷药恩替卡韦美国上市,其效果优于拉米夫定,且耐药率低,一经上市就受到追捧。直到现在,恩替卡韦依旧是治疗慢乙肝的一线治疗药物。虽然恩替卡韦对初治患者效果好,耐药率低,但对使用了拉米夫定且耐药的患者,却相对更容易耐药。
2008年,吉利德旗下核苷药替诺福韦酯获FDA批准用于乙肝(最早2001年上市用于艾滋病)。后来又出现了吉利德的丙酚替诺福韦(TAF,别名富马酸丙酚替诺福韦、富马酸磷丙替诺福韦)、豪森的艾米替诺福韦(TMF,别名艾美酚胺替诺福韦片),都是替诺福韦酯的升级版。这两款药能进入肝细胞胞浆并对肝内病毒复制起效,安全性更高且抗病毒效果更好。
核苷药物的出现,给慢乙肝患者带来了极大的希望,降低了肝硬化、肝癌的发生风险。但可惜的是,无论哪种核苷药物,都难以治愈乙肝,只能抑制病毒复制,减少或延缓病情的进展,且需要长期服药。随着科学技术的进步,人们对干扰素α进行了“升级”,由此诞生了聚乙二醇干扰素α,也就是长效干扰素,它的持续时间更长,效果也更好。随后,聚乙二醇干扰素α-2b上市。2010年左右,当时医学界已经有人发现,经过核苷和聚乙二醇干扰素α联合治疗的患者,会出现HBsAg的清除。后续研究表明,核苷经治优势患者加用聚乙二醇干扰素临床治愈率可达30%-80%。
借助这一发现,2015-2016年,我国《慢乙肝防治指南》首次提出临床治愈的理念。2017-2018年,临床治愈在国内外达成共识,理念获得国际认可。中国慢乙肝临床治愈(珠峰)工程项目启动。2020年,《慢乙肝临床治愈(功能性治愈)专家共识》的发布,明确了聚乙二醇干扰素α在实现慢乙肝患者临床治愈中的地位。2022年,《慢乙肝防治指南》2022版的发布,再次确定了聚乙二醇干扰素α在实现慢乙肝患者临床治愈中的重大意义。
虽然慢性乙肝尚无法治愈,但彻底清除乙肝病毒,实现乙肝病毒学治愈指日可待。
2021年初,吉利德宣布与VirBiotechnology达成一项临床合作,旨在评估和开发功能性治愈慢性乙肝的新型联合治疗策略。
今年年初,歌礼制药宣布其皮下注射PD-L1抗体ASC22(恩沃利抗体)可以实现慢性乙型肝炎功能性治愈的消息也引起广泛关注。
此外,腾盛博药旗下BRII-835、GSK与Ionis联合开发的bepirovirsen也备受瞩目。
鉴于丙肝的“消亡史”,我们有理由相信未来乙肝也可能被治愈。
本图文来源于【药智网】仅供读者参考,著作权、版权归属原创者所有。转载此文是出于传递更多正能量信息之目的,侵权删






 首页
首页

 癌症科普
癌症科普

 癌症种类
癌症种类

 药品百科
药品百科

 肿瘤医院
肿瘤医院

 名医专家
名医专家

 免费试新药
免费试新药

 健康资讯
健康资讯

 癌症新方案
癌症新方案













